Место в котором проходит передняя межжелудочковая артерия
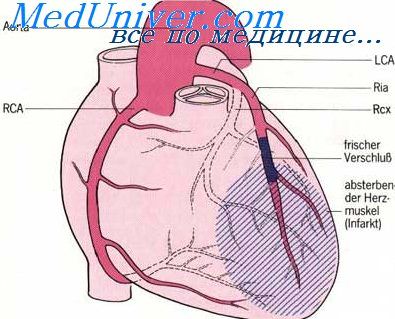
Коронарография с миокардиальным мостиком. В систолической фазе сердечного цикла отмечается сужение диаметра коронарной артерии. В научной литературе данный феномен обозначается как «milking effect» или «step up – step down».
С 2018 года в Национальном медицинском исследовательском центре им. В. А. Алмазова внедрено оперативное лечение миокардиальных мостиков коронарных артерий новым методом супракоронарной миотомии.
За прошедший год кардиохирургами Центра выполнено более двух десятков открытых операций на сердце, в ходе которых проведена коррекция аномального развития коронарных артерий. Миокардиальные мостики — наиболее распространенный вариант данной патологии.
При этом заболевании один из сегментов коронарной артерии (чаще всего средний сегмент передней межжелудочковой артерии) проходит в толще сердечной мышцы, в то время как при нормальном развитии сосудов сердца коронарные артерии располагаются эпикардиально, в толще жировой и соединительной тканей. Такая врожденная аномалия коронарного русла служит одной из причин нарушения кровообращения и приводит к
развитию ишемии миокарда вплоть до некроза.

На рисунке показано интрамиокардиальное расположение коронарной артерии. По результатам многочисленных исследований было выявлено, что миокардиальные мостики способствуют развитию коронарного атеросклероза.
Супрокоронарная миотомия в настоящее время является единственным патогенетически обоснованным и радикальным вариантом лечения миокардиальных мостиков. Суть операции заключается в рассечении мышечных волокон, под которыми располагается артерия, что позволяет исключить компрессию сосуда и изменение его диаметра в зависимости от сердечных сокращений.
Данный вид операций осуществляется лишь в нескольких ведущих медицинских центрах России. В 2018 году в Центре Алмазова их выполнено двадцать три. В шестнадцати случаях применена изолированная супракоронарная миотомия, в пяти — супракоронарная миотомия с коронарным шунтированием и в одном случае потребовалась супракоронарная миотомия с коррекцией клапанной патологии. Однако наибольший интерес вызвал клинический случай супракоронарной миотомии на донорском сердце во время трансплантации сердца.
Важнейшую роль в диагностике и определении показаний к оперативному лечению играют такие исследования, как стресс-эхокардиография, коронарография, позитронно-эмиссионная томография и мультиспиральная компьютерная томография — все эти обязательные методы исследований пациентов с аномальным развитием коронарных артерий в Центре представлены.
Отделения сердечно-сосудистой хирургии тесно сотрудничают с научно-исследовательскими отделами и лабораториями Института сердца и сосудов, а также с НИЛ ядерной медицины. В Центре Алмазова продолжаются исследования, связанные с изучением медикаментозной терапии у данной группы пациентов, информативности различных диагностических подходов, вариантов хирургической
коррекции аномалии. В ближайшее время планируется внедрение миниинвазивных доступов для
выполнения супракоронарной миотомии, а также интраоперационное использование ультразвукового
аппарата нового поколения для облегчения визуализации целевой артерии.
Анализ ближайших и отдаленных результатов хирургического лечения пациентов, прооперированных в Центре Алмазова, подтверждает эффективность и перспективность нового вида лечения миокардиальных мостиков — супракоронарной миотомии
Место в котором проходит передняя межжелудочковая артерия
Анатомия коронарного кровообращения весьма вариабельна. Особенности коронарного кровообращения каждого человека неповторимы, как отпечатки пальцев, поэтому и каждый инфаркт миокарда "индивидуален". Глубина и распространённость инфаркта зависят от переплетения многих факторов, в частности от врождённых анатомических особенностей коронарного русла, степени развития коллатералей, выраженности атеросклеротического поражения, наличия "продромов" в виде стенокардии, впервые возникшей в течение предшествующих инфаркту суток (ишемическая "тренировка" миокарда), спонтанной либо ятрогенной реперфузии и др.
Как известно, сердце получает кровь из двух венечных (коронарных) артерий: правой венечной артерии [a. coronaria dextra — по-латыни или right coronary artery (RCA) — по-английски] и левой венечной артерии [соответственно a. coronaria sinistra и left coronary artery (LCA)]. Это первые ветви аорты, которые отходят от правого и левого её синусов.
Ствол ЛКА [по-английски — left main coronary artery (LMCA)] отходит от верхней части левого синуса аорты и идёт позади лёгочного ствола. Диаметр ствола ЛКА составляет от 3 до 6 мм, протяженность — до 10 мм. Обычно ствол ЛКА делится на две ветви: переднюю межжелудочковую ветвь (ПМВ) и огибающую (рис. 4.11). В 1/3 случаев ствол ЛКА делится не на два, а на три сосуда: переднюю межжелудочковую, огибающую и срединную (промежуточную) ветви. В этом случае срединная ветвь (ramus medianus) располагается между передней межжелудочковой и огибающей ветвями ЛКА.
Этот сосуд — аналог первой диагональной ветви (см. ниже) и обычно снабжает переднебоковые отделы левого желудочка.
Передняя межжелудочковая (нисходящая) ветвь ЛКА следует по передней межжелудочковой борозде (sulcus interventricularis anterior) в направлении верхушки сердца. В англоязычной литературе этот сосуд называют левой передней нисходящей артерией: left anterior descending artery (LAD). Мы будем придерживаться более точного анатомически (F. H. Netter, 1987) и принятого в отечественной литературе термина "передняя межжелудочковая ветвь" (О. В. Федотов и др., 1985; С. С. Михайлов, 1987). В то же время при описании коронарограмм лучше использовать термин "передняя межжелудочковая артерия", чтобы упростить название её ветвей.
Главные ветви последней — перегородочные (проникающие, септальные) и диагональные. Перегородочные ветви отходят от ПМВ под прямым углом и углубляются в толщу межжелудочковой перегородки, где анастомозируют с аналогичными ветвями, отходящими снизу от задней межжелудочковой ветви правой коронарной артерии (ПКА). Эти ветви могут отличаться по количеству, длине, направлению. Иногда встречается крупная первая перегородочная ветвь (идущая либо вертикально, либо горизонтально — как бы параллельно ПМВ), от которой отходят веточки к перегородке. Отметим, что из всех областей сердца межжелудочковая перегородка сердца обладает самой густой сосудистой сетью. Диагональные ветви ПМВ проходят по переднебоковой поверхности сердца, которую и кровоснабжают. Таких ветвей бывает от одной до трёх.
В 3/4 случаев ПМВ не заканчивается в области верхушки, а, огибая последнюю справа, заворачивается на диафрагмальную поверхность задней стенки левого желудочка, кровоснабжая соответственно как верхушку, так и частично заднедиафрагмальные отделы левого желудочка. Именно этим объясняется появление на ЭКГ зубца Q в отведении aVF у больного с обширным передним инфарктом. В остальных же случаях, оканчиваясь на уровне или не доходя до верхушки сердца, ПМВ не играет существенной роли в её кровоснабжении. Тогда верхушка получает кровь от задней межжелудочковой ветви ПКА.
Проксимальным участком передней межжелудочковой ветви (ПМВ) ЛКА называют отрезок от устья этой ветви до отхождения первой перегородочной (проникающей, септальной) ветви или же до отхождения первой диагональной ветви (менее строгий критерий). Соответственно средний участок — это отрезок ПМВ от конца проксимального участка до отхождения второй либо третьей диагональной ветви. Далее располагается дистальный участок ПМВ. Когда есть только одна диагональная ветвь, границы среднего и дистального участков определяются приблизительно.
Артериальный [[боталлов]] проток - Предсердные ветви
Артериальный [[боталлов]] проток
, ductus arteriosus [[Botalli]]. Короткий артериальный ствол между бифуркацией легочного ствола и дугой аорты. Функционирует до рождения. Рис. А.
Артериальная связка
, lig. arteriosum. Фиброзный тяж на месте заросшего артериального протока. Рис. Б.
АОРТА
, aorta. Самый крупный артериальный сосуд большого круга кровообращения. Рис. Б.
ВОСХОДЯЩАЯ ЧАСТЬ АОРТЫ
, pars ascendens aortae. Находится в пределах перикарда и идет в восходящем направлении. Рис. Б.
Луковица аорты
, bulbus aortae. Расширение стенки аорты возле ее основания. Соответствует синусам аорты. Рис. В.
Синусы аорты
, sinus aortae. Расширения просвета аорты на уровне заслонок аортального клапана. Рис. В.
Правая венечная артерия
, a. coronaria dextra. Начинается от правого синуса аорты и проходит в правой венечной борозде. Рис. В, Рис. Г.
Предсердно-желудочковые ветви
, rami atrioventriculares. Расположены в одноименной борозде. Участвуют в кровоснабжении предсердно-желудочкового узла. Рис. Г.
Ветвь артериального конуса
, ramus coni arteriosi. Разветвляется в верхней части правого желудочка. Рис. В.
Ветвь синусно-предсердного узла
, ramus nodi sinoatrialis. Направляется к сосудистому сплетению у отверстия верхней полой вены и далее к синусно-предсердному узлу. Встречается в 55 % случаев. Рис. В.
Предсердные ветви
, rami atriales. Кровоснабжают стенку правого предсердия. Рис. В.
Правая краевая ветвь
, ramus marginalis dexter. Спускается вниз вдоль края правого желудочка. Рис. В, Рис. Г
Промежуточная предсердная ветвь
, ramus atrialis intermedius. Идет в восходящем направлении по задней поверхности правого предсердия. Рис. Г.
Задняя межжелудочковая ветвь
, ramus interventricularis posterior. Конечная ветвь правой венечной артерии в задней межжелудочковой борозде. Рис. Г.
Перегородочные межжелудочковые ветви
, rami interventriculares septales. Кровоснабжают межжелудочковую перегородку. Рис. Г.
Ветвь предсердно-желудочкового узла
, ramus nodi atrioventricularis. Отходит у начала межжелудочковой ветви и направляется к предсердно-желудочковому узлу. Рис. Г.
Правая заднелатеральная ветвь
, ramus posterolateralis dexter]. Кровоснабжает заднюю стенку левого желудочка. Присутствует непостоянно. Рис. Г.
Левая венечная артерия
, а. coronaria sinistra. Короткий ствол, который отходит от левого синуса аорты. Рис. В.
Передняя межжелудочковая ветвь
, ramus interventricularis anterior. Проходит в передней межжелудочковой борозде. Рис. В.
Ветвь артериального конуса
, ramus coni arteriosi. Направляется к артериальному конусу. Рис. В.
Латеральная ветвь
, ramus lateralis. Кровоснабжает переднюю стенку левого желудочка. Рис. В.
Перегородочные межжелудочковые ветви
, rami interventriculares septales. Кровоснабжают передние 2/3 межжелудочковой перегородки. Рис. В.
Огибающая ветвь
, ramus circumflexus. Является продолжением a.coronaria sinistra. Занимает левую часть венечной борозды. Рис. В, Рис. Г.
Анастомотическая предсердная ветвь
, ramus аtrialis anastomoticus. Проходит через межпредсердную перегородку и анастомозирует непосредственно с правой венечной артерией или с одной из ее ветвей. Рис. В.
Предсердно-желудочковые ветви
, rami atrioventriculares. Дистальная часть огибающей ветви, расположенная в sulcus atrioventricularis. Рис. Г.
Левая краевая ветвь
, ramus marginalis sinister. Разветвляется в стенке левого желудочка. Рис. В.
Промежуточная предсердная ветвь
, ramus atrialis intermedius. Кровоснабжает заднюю стенку левого предсердия. Рис. Г.
Задняя ветвь левого желудочка
, ramus posterior ventriculi sinistri. Направляется к задней стенке левого желудочка. Встречается непостоянно. Рис. Г.
Ветвь синусно-предсердного узла
, ramus nodi sinoatrialis]. Встречается в 45% случаев. Отходит у места начала левой венечной артерии и направляется к синусно-предсердному узлу. Рис. В.
Ветвь предсердно-желудочкового узла
, ramus nodi atrioventricularis]. Кровоснабжает предсердно-желудочковый узел. Встречается непостоянно. Рис. Г
Место в котором проходит передняя межжелудочковая артерия
Оказывая помощь при ранениях сердца, хирург должен четко ориентироваться в топографии сосудов сердца, чтобы избежать нарушений его кровоснабжения при ушивании ран.
Артерии, вены и лимфатические сосуды сердца расположены в жировом слое эпикарда. В редких случаях небольшие участки коронарных артерий могут располагаться в глубине миокарда.
Первая и левая коронарные артерии отходят от аорты тотчас над створками клапана, и направляются вперед, охватывая ствол легочной артерии.
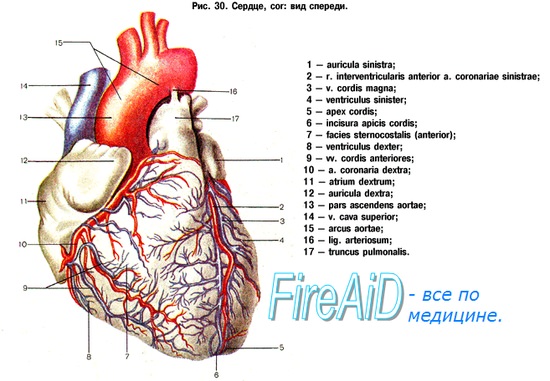
Крупный ствол левой коронарной артерии проходит между стволом легочной артерии и левым предсердием и, достигая предсердно-желудочковой борозды, делится на два крупных ствола — переднюю межжелудочковую артерию (ПМЖА) и огибающую артерию (ОА), которая отдает кзади ветви тупого края.
ПМЖА спускается но межжелудочковой борозде к верхушке сердца, давая диагональные ветви, снабжающие всю переднюю поверхность левого желудочка, часть передней стенки правого желудочка, а также ветви, идущие внутрь, к межжелудочковой перегородке и к передней папиллярной мышце.
Огибающая артерия идет практически горизонтально влево по предсердно-желудочковой борозде и дает многочисленные ветви, снабжающие боковую и заднюю стенки левого желудочка.
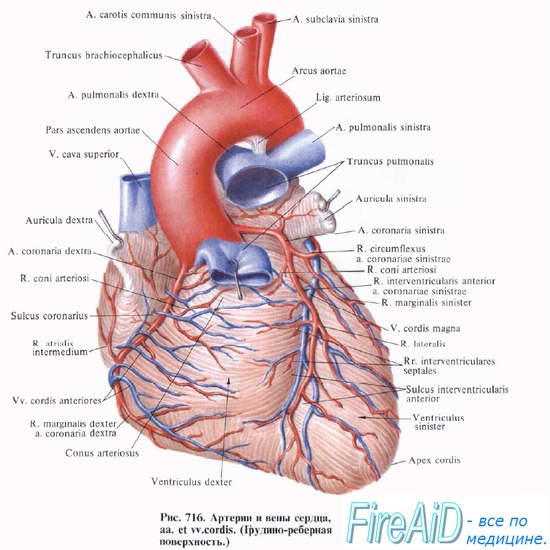
Правая коронарная артерия проходит между правым предсердием и правым желудочком спереди назад, продолжаясь в виде задней межжелудочковой артерии, достигающей верхушки сердца. Она питаетнижние и задние стенки обеих желудочков и заднюю треть межжелудочковой перегородки. Крупные ветви правой коронарной артерии (ветви острого края) — снабжают кровью переднюю стенку правого желудочка.
Коронарные вены следуют по ходу основных коронарных артерий, располагаясь более поверхностно, нежели артерии. Через коронарный синус венозная кровь возвращается в правое предсердие.
Лимфатические сосуды следуют также по ходу коронарных артерий и вен и впадают в крупный лимфатический коллектор средостения, а затем в грудной проток. Впрочем большого значения лимфосистема сердца при его ранении не имеет.
Коронароангиография

В университетскую программу первых курсов входит изучение строения сердца и его коронарных сосудов. Но чаще всего авторы учебников ограничиваются описанием только крупных сосудов. Клиницисты же используют совершенно иную, но также международную номенклатуру. Коронароангиография и имплантация стентов требуют более подробного описания сосудов сердца, что нашло применение и в международной практике.

Из курса анатомии каждый узнал, что от аорты отходят две артерии, кровоснабжающие само сердце: левая и правая коронарные артерии. Утолщения на корне аорты, из которых и выходят эти артерии, называются соответственно левым и правым коронарными синусами.

Выделяют следующие части левой коронарной артерии (LCA, left coronary artery): главный ствол, который делится на переднюю межжелудочковую ветвь (ramus interventricularis anterior, RIVA или left anterior descending, LAD), а также огибающую артерию (left circumflex coronary artery, LCх).
Главный ствол этой артерии длиной редко превышает 1 см, а далее делится на две свои конечные ветви. Передняя межжелудочковая ветвь располагается на передней поверхности сердца вплоть до его верхушки. На своем протяжении от этой артерии отходят передние желудочковые ветви (диагональные ветви, RD/R.Diag) и передние перегородочные ветви. В коронароангиографии с целью топического указания места поражения предложено делить коронарное русло на сегменты.
Проксимальный сегмент ПМЖВ начинается своим ответвлением от ствола и продолжается до места отхождения от нее первой перегородочной или первой RD, средняя часть — до ответвления второй перегородочной ветви или второй RD, дистальная — до верхушки сердца/после отхождения второй RD.

Огибающая артерия всегда располагается на задней поверхности сердца. В ее проксимальной части от нее отходит ветвь тупого края (obtuse marginal artery, obtuse marginal branch, OMB). В зависимости от места этого ответвления различают проксимальную и дистальную части огибающей ветви. Очень редко от главного ствола между передней межжелудочковой ветвью и огибающей ветвью посередине отходит еще одна ветвь, берущая начало непосредственно из общего ствола — промежуточная артерия (RIM, ramus intermedius).
Выделяют следующие три части правой коронарной артерии (RCA): проксимальную (от устья до первого ее поворота, обычно располагающегося горизонтально), среднюю (от первого до второго поворота) и дистальную (после второго ее поворота до разделения артерии на ветви у «креста» сердца (crux cordis) — места пересечения задней межжелудочковой и атриовентрикулярной борозд сердца). Иногда непосредственно после самого устья от сосуда отходит маленькая ветвь — ветвь артериального конуса (ramus coni arteriosi, CB), а также много мелких ветвей к правому предсердию.
Самой главной из этих ветвей является артерия синоатриального узла (S-A node artery, SNA). Она часто располагается под правым ушком сердца. В редких случаях ветвь артериального конуса имеет собственное устье. Этот вариант всегда следует учитывать, поскольку при коронароангиографии можно принять эту артерию за главный ствол правой коронарной артерии. Перекрыв вход в эту артерию катетером, можно вызвать локальную ишемию и, как следствие, нарушения ритма вплоть до трепетания камер сердца. В передней части венечной борозды, в области острого края сердца, от правой коронарной артерии отходит ветвь острого края (acute marginal artery, AMB), чаще от одной до трех, которая в большинстве случаев достигает верхушки сердца.
Итак, перечислим еще раз все сокращения:
Левая коронарная артерия — left coronary artery (LCA):
— Передняя межжелудочковая ветвь (ПМЖВ), или передняя нисходящая артерия — left anterior descending artery (LAD); иначе — ramus interventricularis anterior (RIVA/RIA);
— Диагональные артерии (ветви) — ДА; ramus diagonalis (RD/Diag);
— Огибающая ветвь (ОВ) левой коронарной артерии, огибающая артерия — left circumflex coronary artery (LCх));
— Ветвь тупого края, obtuse marginal artery, obtuse marginal branch, (OMB);
— Перегородочные межжелудочковые ветви, ramus septalis (RSA);
— Промежуточная артерия, ramus intermedius (RIM).
Правая коронарная артерия — right coronary artery (RCA):
— Ветвь острого края, acute marginal artery, (AMB);
— Артерия синоатриального узла — ramus nodi sinuatrialis (S-A node artery, SNASA/RNS);
— Задняя межжелудочковая ветвь (ЗМЖВ), или задняя нисходящая артерия — posterior descending artery (PDA); иначе — ramus interventricularis posterior (RIVP/RIP).
И еще раз для повторения (важное задание для диагностики локализации ишемии при инфаркте миокарда): LAD/RIVA, LCx кровоснабжает левую камеру спереди и сбоку, а RCA — сзади. Левое предсердие кровоснабжают LCx, RCA. Перегородку — RSA от LAD. Правую камеру сзади — RCA, спереди — RCA, LAD. Правое предсердие — RCA.

Следует также напомнить о доминантности кровоснабжения миокарда. При так называемом правом типе кровоснабжения сердца, наблюдающемся у 70 % людей, задняя нисходящая артерия (PDA) отходит от правой коронарной артерии. При левом типе кровоснабжения сердца (10 % людей) огибающая артерия (LCx) достигает уровня задней межжелудочковой борозды и образует заднюю нисходящую артерию (PDA). При еще более редком, так называемом смешанном содоминантном типе (20 % людей), имеются две задних желудочковых ветви (RIVP/RIP), отходящих от правой венечной и огибающей артерий.
Для понимания принципа работы ЭКГ необходимо повторить строение проводящей системы сердца. Синоатриальный узел находится в стенке правого предсердия, его импульсы поступают к атриовентрикулярному узлу (также располагается в стенке правого предсердия). Далее импульс распространяется по волокнам пучка Гиса, который делится в межжелудочковой перегородке на две ножки - правую и левую (иногда называются ножками Тавары). К эндокарду сигнал поступает посредством волокон Пуркинье. Иногда встречаются и дополнительные пути передачи возбуждения, как, например, по волокнам Кента. Такие пути часто располагаются между предсердиями и желудочками и идут в обход атриовентрикулярного узла. Из-за этого мускулатура миокарда часто сокращается преждевременно, что становится заметно на ЭКГ, а такие пациенты предрасположены к тахикардии (WPW-синдром).
Электрокардиограмма представляет собой не что иное, как запись распространяемых электрических потенциалов сердца, фиксируемых электродами на конечностях и грудной стенке. ЭКГ включает в себя три стандартных отведения по Эйнтховену (I, II, III), и три усиленных по Гольдбергу (aVR, aVL, aVF). Прикрепление еще шести грудных электродов по Вильсону (V1-V6) позволяет зарегистрировать распространение возбуждение по сердечной стенке в горизонтальной проекции. В зависимости от изменений в этих отведениях еще на догоспитальном этапе при помощи ЭКГ можно предположить локализацию инфаркта и возможную «проблемную» артерию.
Например, при инфаркте правых отделов сердца (задней стенки) часто особенно сильно поражается правый желудочек. Чаще всего это происходит из-за тромба в RCA. Правые отделы сердца не способны сокращаться должным образом, что приводит к снижению преднагрузки левой камеры сердца, поскольку таким образом снижается объем крови, транспортируемый к левому предсердию. Сниженный сердечный выброс сердце пытается компенсировать увеличением частоты сокращений. При инфаркте же левых отделов сердца основным осложнением является кардиогенный шок.
Специально для наших подписчиков мы сделали таблицу, в которой показаны изменения ЭКГ в зависимости от локализации возможного повреждения коронарных артерий.

Стоит также повторить и классификацию острых коронарных синдромов:
- Нестабильная стенокардия без повышения тропонина. Эта форма классифицируется по Браунвальду на 3 класса в зависимости от выраженности клинических признаков:
I — недавно возникшая боль за грудиной (менее 2-х месяцев, более 3-х раз в день);
II — боль за грудиной в покое (минимум один раз за прошедший месяц, но не в течении последних 48 часов);
III — боль за грудиной в покое (минимум один раз за последний 48 часов).
Нестабильную стенокардию классифицируют на 3 группы по причинам возникновения:
А — вторичная нестабильная стенокардия (инфаркт миокарда, анемия, повышение температуры, гипотензия, тахиаритмия, тиреотоксикоз, дыхательная недостаточность);
B — первичная нестабильная стенокардия;
C — нестабильная стенокардия после инфаркта (минимум 2 недели после инфаркта).
- Инфаркт миокарда без элевации сегмента ST (NSTEMI) с повышением концентрации кардиального тропонина в крови.
ПБКА и стентирование
При ПБКА баллонный катетер с помощью проводника вводится вплоть до места стеноза. Баллон раздувается и тем самым «сплющивает» атеросклеротические бляшки, растягивая сосудистую стенку. Мелкие повреждения интимы во время раздувания баллона часто не имеют последствий, однако иногда именно в этих местах позже начинается пролиферация тканей, что в 30–40 % случаев приводит к рестенозам и рецидивам в течение последующих трех месяцев. Частота экстренных операций по созданию шунтов (bypass) составляет менее 0,5 %. С помощью имплантации стента сосудистая стенка стабилизируется. Существовала также техника primary stenting — имплантация стента без предшествующего дилатирования сосудов баллоном, однако ныне она используется крайне редко и только на начальных этапах сужения просвета сосуда. Исследования последних лет показали, что при значительных сужениях просвета сосуда, у таких пациентов в первые часы после ангиопластики наблюдалась ишемия миокарда, что требовало немедленного повторного хирургического вмешательства или повторной дилатации. Это осложнение возникает вследствие отрыва бляшки от эндотелия. Обнажение поверхности гладкомышечных клеток приводит к тромбообразованию за счет высвобождения молекул коллагена и тканевых факторов, запускающих каскад свертывания крови. Во избежание развития тромбов и рестеноза в настоящее время чаще всего ангиопластику совмещают с имплантацией стентов на месте стеноза.
Первую имплантацию стента провел Sigwart в 1987 году. Тогда стенты монтировались непосредственно на баллон самим врачом. Сейчас же вся конструкция идет в комплекте, что позволило снизить риск потери стента в кровеносном русле при его недостаточной фиксации.

Появились и новые типы самих баллонов. Некоторые из них имеют на своей поверхности режущие зубцы, что расположены параллельно оси сосуда, а также баллоны из нитинола и нейлона хеликальные или же параллельные оси сосуда. Эти конструкции позволяют создать идеальную площадку для имплантации будущего стента. Сперва в процессе исследований ученые не заметили разницы между такими баллонами и стандартными, однако недавно выяснилось, что такие надсекающие баллоны, покрытые лекарственными средствами, показывают лучшие результаты.

Различают два типа металлических стентов: саморасширяющиеся и прикрепленные к дилатирующему баллону. Исследования показывают, что применение первого типа стентов чаще вызывает развитие неоинтимальной гиперплазии. Поэтому в настоящее время часто используются стенты второго типа. Как правило, они состоят из металлической трубочки, в которой с использованием различных техник создаются отверстия. После расширения сосуда баллонным катетером в его просвете создается сеть, обволакивающая его стенки изнутри. Прототипом такого типа стентов являлся стент Palmaz-Schatz, который сейчас уже не применяется.
Исследование 1994 года не показало разницы между имплантацией такого стента и обычной ангиопластикой. Развитие этого направление позволило разработать новые типы стентов. Чаще всего они состоят из нескольких модулей, соединенных коннекторами. Изначально их производили из стали, однако сейчас в качестве материала для изготовления стентов используется платина, кобальт, нитинол (никель-титан), а также только титан. Из-за этого они стали существенно меньше и легче. РКИ выявили преимущества стентов с толстым каркасом перед таковыми с тонким. Предполагают, что они меньше травмируют сосуды, предотвращая таким образом реэндотелизацию.

Существуют также стенты с особым покрытием, создающим непроницаемый для крови барьер. К таким вещества относят политетрафторэтилен и полиэтилен. Сперва их использовали для экстренного закрытия небольших перфораций коронарных артерий, однако сейчас их применяют в профилактике коронарных аневризм и артериовенозных фистул.
Drug-eluting-stents (DES) покрыты специальными веществами, подавляющими пролиферацию клеток эндотелия, таким образом препятствуя рестенозированию сосуда, чаще всего развивающемуся в течение 4–8 месяцев после имплантации.
Стенты – ферромагнетики, плотно устанавливающиеся в сосудистом русле не являются противопоказанием для проведения МРТ.

Существуют специальные стенты для позиционирования их в устьях и разветвлениях сосудов. Как и любой инородный объект в кровеносном русле, стенты являются дополнительным фактором тромбообразования. Поэтому после самой процедуры пациенту всегда назначают ДААТ или ТАТ.
Брахитерапия
Этот метод основан на радиоактивном облучении коронарных артерий при рецидивах после имплантации стентов. Для этого используется бета-излучение, поскольку оно способно проникать лишь на несколько миллиметров внутрь толщи ткани. При этом методе катетер вводят в место стеноза, который прежде был дилатирован баллоном. С помощью этого катетера зону определенное количество времени (3–5 минут) облучают рассчитанной дозой. Васкулярная брахитерапия используется с 1996 года. В феврале 2005 года прекратила свое существование фирма, разрабатывающая аппараты для брахитерапии коронарных сосудов (Beta-Cath-System).

Ротаблационная пластика
Этот метод используется с 1989 года. В сосуд вводится алмазный бор, способный вращаться с частотой 190 000 об. в минуту. С его помощью удаляются ткани в месте рестенозирования. Величина таким образом измельченных частиц составляет 5–10 микрометров (длина эритроцита — 7,5 микрометров). Образуемый канал очень небольшой в диаметре, но достаточный для проведения ПТКА. Как правило, метод используют в случае образования на месте рестеноза кальцификатов. Диаметр головки бора варьируется от 1,25 до 2,5 мм. Поскольку кабель для ротаблационного бора плохо проходит место стеноза, успех операции составляет 80–95 %. К осложнениям относят спазмы сосудов, возникающие чаще (5 %), чем при ПТКА.

Интраваскулярный ультразвук
Еще одним инструментом кардиолога является метод интраваскулярного ультразвука (IVUS). В сосуд вводят ультразвуковой зонд.
Порядок манипуляций напоминает таковой при ПТКА: после позиционирования проводника зонд проводят к месту стеноза. Ультразвук позволяет просмотреть 1 мм тканей на расстоянии от излучателя. Всего на верхушке катетера используется 64 таких кристалла (пьезоэлемента). С помощью этого метода возможно определить состав бляшек и их фибринные, липидные и кальциевые составляющие. Чаще всего к ультразвуку прибегают при неоднозначности ангиографической картины, используя как дополнительный метод обследования.

Всех нас на физиологии мучили графиками давления в сосудах. Мало кто на младших курсах мог подумать, что эти данные действительно используются в диагностике. При каждой коронароангиографии исследуют давление в коронарных артериях и его изменения в зависимости от наличия стенозированных участков. Для этого к исследуемому участку подводят детектор диаметром 0,014 дюймов. Этот катетер продвигают до самого конца коронарной артерии. Потом его тянут обратно. Таким образом фиксируется давление на всем протяжении артерии. На мониторе врачи наблюдают изменение давления; в месте наибольшего его перепада чаще всего и оказывается самый стенозированный участок. Постепенное изменение давления является свидетельством диффузного заболевания сосудов. Важно откалибровать детектор до самого исследования. После аппликации аденозина наблюдается гиперемия, то есть увеличение циркуляции крови, что симулирует состояние нагрузки. После этого давление на протяжении сосуда измеряется еще раз, что позволяет определить, являются ли места стенозирования важными, вызывают ли именно они боли у пациента при физических нагрузках. Аденозиновый тест не является безопасным: возможно развитие нарушений сердечного ритма, однако из-за короткого периода полувыведения аденозина лишь кратковременно.
Спазмы коронарных сосудов и ацетилхолиновый тест
Спазмы коронарных артерий часто являются причиной болей за грудиной в ночное время суток у пациентов без видимых изменений коронарных сосудов. Таким пациентам также назначают коронароангиографию и проводят вышеуказанный провокационный тест, чтобы исключить психогенные или некардиальные причины таких симптомов. Сейчас у каждого человека, уже сдавшего физиологию, должна промелькнуть мысль: «Почему ацетилхолин?». Если вы не находите ответа, возможно, придется снова открыть учебник. Дело в том, что эндотелий сердца при аппликации ацетилхолина вырабатывает NO, что приводит к расширению сосудов. Ацетилхолин оказывает вазоконстрикторное действие на гладкомышечные клетки сосудов в результате прямой их стимуляции, если эндотелий поврежден. Таким образом можно отличить здоровый эндотелий от поврежденного. Здоровые сосуды реагируют на ацетилхолин расширением, поврежденные же сужаются. При сужении сосудов более чем на 75 % по сравнению с аппликацией нитроглицерина внутрикоронарно говорят о коронарном спазме.
Учебное видео кровоснабжения сердца (анатомии артерий и вен)
При проблемах с просмотром скачайте видео со страницы ЗдесьРедактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Артерии
Сердце
, pericardium. Отграничивает сердце от соседних органов. Состоит из фиброзного и двух листков серозного перикарда. Рис. А.
Фиброзный перикард
, pericardium fibrosum. Плотная наружная соединительнотканная часть перикарда. Частично срастается с диафрагмой.
Грудино-перикардиальные связки
, ligg. sternopericardiaca. Соединяют перикард с грудиной.
Серозный перикард
, pericardium serosum. Состоит из однослойного плоского эпителия (мезотелия). С одной стороны прилежит к фиброзному перикарду (париетальная пластинка), с другой - покрывает сердце (висцеральная пластинка). В области крупных сосудов пластинки переходят одна в другую.
Париетальная пластинка
, lamina parietalis. Часть серозного перикарда.
Висцеральная пластинка [эпикард]
, lamina visceralis [epicardium]. Cостоит из мезотелия и слоя рыхлой волокнистой соединительной ткани (lamina propria).
Перикардиальная полость
, cavitas pericardialis. Находится между двумя листками cерозного перикарда и содержит небольшое количество жидкости.
Поперечная пазуха перикарда
, sinus transversus pericardii. Расположена между аортой и легочным стволом сзади, легочными венами спереди. Рис. А.
Косая пазуха перикарда
, sinus obliquus pericardii. Ограничена основаниями правых легочных вен и v. cava inferior с одной стороны, левыми легочными венами - с другой. Рис. А.
СЕРДЦЕ
Основание сердца
, basis cordis. Его широкая верхняя поверхность направлена дорсально, в сторону, противоположную верхушке. Она образована, главным образом, задней стенкой левого предсердия.
Грудино-реберная [передняя] поверхность
, facies sternocostalis [anterior]. Выпуклая, направленная вперед поверхность сердца. Рис. Б, Рис. Г.
Диафрагмальная поверхность [нижняя]
, facies diaphragmatica [inferior]. Нижняя, плоская поверхность сердца, которая соприкасается с диафрагмой. Рис. Г.
Легочная поверхность
, facies pulmonalis. Соприкасается с легкими. Рис. Г.
Правый край
, margo dexter. У трупа обычно заостренный. Рис. Б.
Верхушка сердца
, apex cordis. Направлена вперед, вниз и влево. Рис. Б.
Вырезка верхушки сердца
, incisura apicis cordis. Находится с правой стороны от верхушки сердца в месте соединения межжелудочковых борозд. Рис. Б.
Передняя межжелудочковая борозда
, sulcus interventricularis anterior. Расположена на передней поверхности сердца и соответствует межжелудочковой перегородке. В ней проходит передняя межжелудочковая ветвь левой венечной артерии. Рис. Б, Рис. Г.
Задняя межжелудочковая борозда
, sulcus interventricularis posterior. Проходит по диафрагмальной поверхности сердца и соответствует межжелудочковой перегородке. Содержит заднюю межжелудочковую ветвь правой венечной артерии. Рис. Г.
Венечная борозда
, sulcus coronarius. Огибает сердце на границе между предсердиями и желудочками. Рис. Б, Рис. В.
Желудочек сердца [правый/левый]
, ventriculus [dexter/sinister] cordis. Отвечая функциональным потребностям, стенка левого желудочка толще, чем правого. Рис. В.
Межжелудочковая перегородка
, septum interventriculare. Разделяет правый и левый желудочек. На поверхности сердца ей соответствуют передняя и задняя межжелудочковые борозды.
Мышечная часть
, pars muscularis. Наиболее протяженная и толстая часть межжелудочковой перегородки. Рис. В.
Перепончатая часть
, pars membranacea. Небольшой протяженности тонкая фиброзная пластинка в составе межжелудочковой перегородки, расположенная выше отверстия аорты. Производное эндокарда. Рис. В.
Предсердно-желудочковая перегородка
, septum atrioventriculare. Участок перепончатой части межжелудочковой перегородки, расположенный выше основания перегородочной створки трехстворчатого клапана между правым предсердием и левым желудочком. Рис. В.
Предсердие [правое/левое]
, atrium [dextrum/sinistrum] cordis. Тонкостенная камера сердца. Рис. В.
Ушко предсердия
, auricula atrialis. Пальцевидное выпячивание стенки правого и левого предсердий. Рис. Б, Рис. В.
Межпредсердная перегородка
, septum interatriale. Проходит между правым и левым предсердиями.
Предсердно-желудочковое отверстие (правое/левое)
, ostium atrioventriculare (dexter/sinister). Находится между предсердием и желудочком. Рис. Г.
Отверстие легочного ствола
, ostium trunci pulmonalis. Соединяет правый желудочек с легочным стволом. Рис. Г.
Отверстие аорты
, ostium aortae. Соединяет левый желудочек с аортой. Рис. В, Рис. Г.
Анатомия сердечно-сосудистой системы
1. Правая коронарная артерия
2. Передняя нисходящая артерия
3. Ушко
4. Верхняя полая вена
5. Нижняя полая вена
6. Аорта
7. Лёгочная артерия
8. Ветви аорты
9. Правое предсердие
10. Правый желудочек
11. Левое предсердие
12. Левый желудочек
13. Трабекулы
14. Хорды
15. Трикуспидальный клапан
16. Митральный клапан
17. Клапан лёгочной артерии
Для того чтобы говорить о заболеваниях сердечно-сосудистой системы необходимо представлять её строение. Кровеносная система делится на артериальную и венозную. По артериальной системе кровь течёт от сердца, по венозной - притекает к сердцу. Различают большой и малый круг кровообращения.
Большой круг включает в себя аорту (восходящая и нисходящая, дуга аорты, грудной и брюшной отдел), по которой течёт кровь от левых отделов сердца. От аорты кровь попадает в сонные артерии, кровоснабжающие головной мозг, подключичные артерии, кровоснабжающие руки, почечные артерии, артерии желудка, кишечника, печени, селезёнки, поджелудочной железы, органов малого таза, подвздошные и бедренные артерии, кровоснабжающие ноги. От внутренних органов кровь оттекает по венам, которые впадают в верхнюю полую вену (собирает кровь от верхней половины туловища) и нижнюю полую вену (собирает кровь от нижней половины туловища). Полые вены впадают в правое сердце.
Малый круг кровообращения включает в себя лёгочную артерию (по которой, тем не менее, течёт венозная кровь). По лёгочной артерии кровь поступает в лёгкие, где обогащается кислородом и становиться артериальной. По лёгочным венам (четыре) артериальная кровь поступает в левое сердце.
Перекачивает кровь сердце - полый мышечный орган, состоящий из четырёх отделов. Это правое предсердие и правый желудочек, составляющие правое сердце и левое предсердие и левый желудочек, составляющие левое сердце. Богатая кислородом кровь, поступающая из лёгких по лёгочным венам попадает в левое предсердие, из него - в левый желудочек и далее в аорту. Венозная кровь по верхней и нижней полой венам попадает в правое предсердие, оттуда в правый желудочек и далее по лёгочной артерии в лёгкие, где обогащается кислородом и снова поступает в левое предсердие.
Различают перикард, миокард и эндокард. Сердце расположено в сердечной сумке - перикарде. Сердечная мышца - миокард состоит из нескольких слоёв мышечных волокон, в желудочках их больше чем в предсердиях. Эти волокна, сокращаясь, проталкивают кровь из предсердий в желудочки и из желудочков в сосуды. Внутренние полости сердца и клапаны выстилает эндокард.
Клапанный аппарат сердца
Между левым предсердием и левым желудочком находится митральный (двухстворчатый) клапан, между правым предсердием и правым желудочком - трикуспидальный (трёхстворчатый). Аортальныё клапан находится между левым желудочком и аортой, клапан лёгочной артерии - между лёгочной артерией и правым желудочком.
Работа сердца
Из левого и правого предсердия кровь поступает в левый и правый желудочек, при этом митральный и трикуспидальный клапан открыты, аортальный и клапан лёгочной артерии закрыты. Эта фаза в работе сердца называется диастолой. Затем митральный и трикуспидальный клапаны закрываются, желудочки сокращаются и через открывшиеся аортальный и клапан лёгочной артерии кровь, соответственно, устремляется в аорту и лёгочную артерию. Эта фаза называется систолой, систола короче диастолы.
Проводящая система сердца
Можно сказать, что сердце работает автономно - само генерирует электрический импульс, который распространяется по сердечной мышце, заставляя её сокращаться. Импульс должен вырабатываться с определённой частотой - в норме около 50-80 импульсов в минуту. В проводящей системе сердца различаю т синусовый узел (находится в правом предсердии), от него идут нервные волокна к атрио-вентрикулярному (предсердно-желудочковому) узлу (расположен в межжелудочковой перегородке - стенке между правым и левым желудочками). От атрио-вентрикулярного узла нервные волокна идут крупными пучками (правая и левая ножка Гиса), делящимися в стенках желудочков на более мелкие (волокна Пуркинье). Электрический импульс генерируется в синусовом узле и по проводящей системе распространяется в толще миокарда (сердечная мышца).
Кровоснабжение сердца
Как и все органы сердце должно получать кислород. Доставка кислорода осуществляется по артериям, которые называются коронарными. Коронарные артерии (правая и левая) отходят от самого начала восходящей аорты (в месте отхождения аорты от левого желудочка). Ствол левой коронарной артерии делиться на нисходящую артерию (она же передняя межжелудочковая) и огибающую. Эти артерии отдают веточки - артерия тупого края, диагональные и др. Иногда от ствола отходит так называемая срединная артерия. Ветви левой коронарной артерии кровоснабжают переднюю стенку левого желудочка, большую часть межжелудочковой перегородки, боковую стенку левого желудочка, левое предсердие. Правая коронарная артерия кровоснабжает часть правого желудочка и заднюю стенку левого желудочка.
Теперь, когда Вы стали специалистом в области анатомии сердечно-сосудистой системы перейдём к её заболеваниям.
Тромбоэмболии - закупорка кровеносных сосудов тромбами. Наиболее опасна тромбоэмболия лёгочной артерии и её ветвей.
Читайте также:


